Importation du produit autorisé aux États-Unis Vasopressine injectable, USP, 20 unités/mL (pour perfusion i.v.) en raison de la pénurie actuelle du produit autorisé au Canada Vasopressine injectable, USP, 20 unités/mL (pour administration i.m. ou s.c.)
Résumé
Voir les messages clés ci-dessous
Produits visés
| Nom de marque du produit |
Forme pharmaceutique, teneur et conditionnement |
Pays ayant délivré l’autorisation de mise en marché et code d’identification | Fabricant | Importateur au Canada |
|---|---|---|---|---|
|
Vasopressine injectable, USP |
Solution aqueuse stérile pour perfusion i.v. (doit être diluée avant l’utilisation); |
États-Unis Chaque fiole : Fiole à dose unique de 1 mL Unité de vente : NDC 63323- |
Fresenius Kabi USA, LLC |
Fresenius Kabi Canada Ltd. |
Problème
Le Canada fait face à une pénurie de Vasopressine injectable, USP, 20 unités/mL (pour administration intramusculaire [i.m.] ou sous-cutanée [s.c.]). Cette pénurie pose des risques graves pour les patients qui pourraient avoir besoin d’un traitement par vasopressine dans un contexte de soins intensifs, selon le jugement clinique de professionnels de la santé qualifiés. Compte tenu du besoin médical, Santé Canada a autorisé l’importation et la vente temporaires et exceptionnelles d’un produit similaire, mais pas identique, de Fresenius Kabi USA, LLC autorisé aux États-Unis, la Vasopressine injectable, USP, 20 unités/mL (pour perfusion intraveineuse [i.v.]) comportant uniquement des étiquettes en anglais.
Destinataires
Professionnels de la santé, y compris les urgentologues, les intensivistes, les anesthésiologistes, les infirmières et infirmières praticiennes, les infirmières en soins critiques et les pharmaciens.
Messages clés
- Le Canada fait face à une pénurie de Vasopressine injectable, USP, 20 unités/mL (pour administration intramusculaire [i.m.] ou sous-cutanée [s.c.]) (DIN 02139502). Compte tenu des risques graves posés par cette pénurie pour les patients en soins intensifs, Santé Canada a autorisé l’importation et la vente temporaires et exceptionnelles d’un produit similaire, mais pas identique, de Fresenius Kabi USA, LLC autorisé aux États-Unis, la Vasopressine injectable, USP, 20 unités/mL (pour perfusion intraveineuse [i.v.]) comportant uniquement des étiquettes en anglais.
- Les professionnels de la santé sont avisés de ce qui suit :
- Il convient de noter que le produit autorisé aux États-Unis, la Vasopressine injectable, USP (pour perfusion i.v.), diffère considérablement du produit autorisé au Canada, la Vasopressine injectable, USP (pour administration i.m. ou s.c.), sur le plan des indications, de la voie d’administration, du conditionnement et de la formulation, des exigences de dilution, des conditions de conservation et des périodes d’utilisation, ainsi que des renseignements en matière d’innocuité (voir la section « Information à l’intention des professionnels de la santé »).
- Il convient de noter que le produit autorisé aux États-Unis est destiné exclusivement à la perfusion intraveineuse après dilution. Il n’est pas indiqué pour une utilisation par voie intramusculaire (i.m.) ou sous-cutanée (s.c.) et l’innocuité de l’administration par voie i.m. ou s.c. n’a pas été établie.
- Consulter les Renseignements d’ordonnance des États-Unis, disponibles en anglais et en français sur le site Web de Fresenius Kabi Canada Ltd., ainsi que les étiquettes intérieures et extérieures autorisées aux États-Unis (voir l’annexe 1), pour obtenir des instructions complètes sur l’utilisation adéquate du produit autorisé aux États-Unis, la Vasopressine injectable, USP (pour perfusion i.v.), y compris les indications, la voie d’administration, la dilution, la posologie, la conservation, les contre-indications, les mises en garde et précautions, ainsi que d’autres renseignements importants.
Contexte
Au Canada, la Vasopressine injectable, USP, 20 unités/mL, est autorisée en vue d’une administration par voie intramusculaire (i.m.) ou sous-cutanée (s.c.) pour la prévention et le traitement de la distension abdominale postopératoire, en roentgénographie abdominale pour dissiper les images de gaz interférents, et dans le diabète insipide. Santé Canada sait que le produit autorisé au Canada a également été utilisé hors indication pour traiter le choc vasodilatateur.
Aux États-Unis, la Vasopressine injectable, USP, 20 unités/mL (pour perfusion i.v.) est indiquée pour augmenter la pression artérielle chez les adultes en choc vasodilatateur qui restent hypotensifs malgré l’administration de liquides et de catécholamines.
Information à l’intention des professionnels de la santé
Le produit autorisé aux États-Unis contient le même ingrédient actif (vasopressine) et la même concentration (20 unités/mL) que le produit de Fresenius Kabi Canada Ltd. autorisé au Canada, la Vasopressine injectable, USP (DIN 02139502). Cependant, il convient de noter qu’il existe des différences importantes sur le plan des indications, de la voie d’administration, du conditionnement et de la formulation, des exigences de dilution, ainsi que des conditions de conservation et des périodes d’utilisation (voir le Tableau 1). Les produits autorisés au Canada et aux États-Unis présentent également des différences en ce qui concerne les renseignements en matière d’innocuité, y compris les contre-indications, les mises en garde et précautions importantes, les effets indésirables et les interactions médicamenteuses, lesquels sont détaillés dans leurs renseignements posologiques respectifs.
Tableau 1 : Principales différences entre le produit autorisé aux États-Unis, la Vasopressine injectable, USP, 20 unités/mL (pour perfusion i.v.) et le produit autorisé au Canada, la Vasopressine injectable, USP, 20 unités/mL (pour administration i.m. ou s.c.).
|
|
|||
|---|---|---|---|---|
| Indication(s) | Augmentation de la pression artérielle chez les adultes en choc vasodilatateur qui restent hypotensifs malgré l’administration de liquides et de catécholamines. | Prévention et traitement de la distension abdominale postopératoire, en roentgénographie abdominale pour dissiper les images de gaz interférents, et dans le diabète insipide. | ||
| Voie d’administration | Pour perfusion intraveineuse (i.v.) uniquement. Doit être diluée avant la perfusion. | Pour injection intramusculaire (i.m.) ou sous-cutanée (s.c.). | ||
| Conditionnement et formulation |
Fiole à dose unique. La solution de 1 mL contient 20 unités/mL de vasopressine, 1,36 mg de tampon d’acétate de sodium et de l’eau pour injection, USP. L’hydroxyde de sodium et l’acide chlorhydrique sont inclus pour régler le pH à 3,8. Sans agent de conservation. |
Fiole à usage multiple. Le bouchon n’est pas fabriqué en latex de caoutchouc naturel. Chaque mL contient : 20 unités USP de vasopressine; 5 mg de chlorobutanol (anhydre) comme agent de conservation; eau pour injection q.s.; acide acétique glacial et/ou hydroxyde de sodium pour régler le pH (2,5 à 4,5). |
||
| Exigences de dilution | Dilution requise avant la perfusion i.v. : diluer à 0,1 ou 1 unité/mL dans une solution saline normale (chlorure de sodium à 0,9 %) ou dans du dextrose à 5 % dans de l’eau. | Aucune dilution n’est nécessaire pour l’administration par voie i.m./s.c. | ||
| Période de conservation et d’utilisation | Conserver les fioles non ouvertes à une température comprise entre 2 °C et 8 °C (peuvent être utilisées jusqu’à la date de péremption du fabricant) ou entre 20 °C et 25 °C (peuvent être utilisées pendant 12 mois ou jusqu’à la date de péremption du fabricant, selon la première éventualité). Ne pas congeler. Pour la solution i.v. diluée : jeter toute solution diluée non utilisée après 18 heures lorsqu’elle est conservée à température ambiante ou après 24 heures lorsqu’elle est réfrigérée. |
Conserver entre 15 °C et 30 °C; jeter dans les 14 jours suivant la première utilisation (fiole à usage multiple). Ne pas laisser congeler. |
Les professionnels de la santé sont avisés de ce qui suit :
- Il convient de noter que le produit autorisé aux États-Unis, la Vasopressine injectable, USP, 20 unités/mL (pour perfusion i.v.) diffère considérablement du produit autorisé au Canada, la Vasopressine injectable, USP, 20 unités/mL (pour administration i.m. ou s.c.) sur le plan des indications, de la voie d’administration, du conditionnement et de la formulation, des exigences de dilution, des conditions de conservation et des périodes d’utilisation, ainsi que des renseignements en matière d’innocuité.
- Le produit autorisé aux États-Unis est destiné exclusivement à la perfusion intraveineuse après dilution. Il n’est pas indiqué pour une utilisation par voie intramusculaire (i.m.) ou sous-cutanée (s.c.) et l’innocuité de l’administration par voie i.m. ou s.c. n’a pas été établie.
- Consulter les Renseignements d’ordonnance des États-Unis, disponibles en anglais et en français sur le site Web de Fresenius Kabi Canada Ltd., ainsi que les étiquettes intérieures et extérieures autorisées aux États-Unis (voir l’annexe 1), pour obtenir des instructions complètes sur l’utilisation adéquate du produit autorisé aux États-Unis, la Vasopressine injectable, USP, 20 unités/mL (pour perfusion i.v.), y compris les indications, la voie d’administration, la dilution, la posologie, la conservation, les contre-indications, les mises en garde et précautions, ainsi que d’autres renseignements importants.
Des images du produit autorisé aux États-Unis, la Vasopressine injectable, USP, se trouvent à l’annexe 1. Ces images sont uniquement en anglais et ne comportent pas de texte en français. Les professionnels de la santé sont avisés que les étiquettes et le conditionnement du produit peuvent différer de ceux du produit autorisé au Canada. Le choix du produit requis doit être vérifié pour éviter toute confusion avec d’autres produits ainsi que pour prévenir des erreurs médicamenteuses.
De plus, le produit autorisé aux États-Unis ne possède pas de numéro d’identification du médicament (DIN) ni de code à barres pouvant être numérisé à l’aide des systèmes de gestion des médicaments au Canada. L’utilisation d’un autocollant généré par l’établissement est recommandée pour permettre le balayage de codes à barres, ainsi que l’identification adéquate du produit distribué et administré. Il incombe à l’organisation réceptrice de produire cet autocollant.
Mesures prises par Santé Canada
Pour aider à pallier le manque de Vasopressine injectable, USP au Canada, Santé Canada a autorisé l’importation et la vente temporaires et exceptionnelles du produit de Fresenius Kabi USA, LLC autorisé aux États-Unis, la Vasopressine injectable, USP, et a ajouté ce produit à la Liste des drogues destinées aux importations et aux ventes exceptionnelles.
Santé Canada a travaillé avec Fresenius Kabi Canada Ltd. pour préparer cette alerte concernant la Vasopressine injectable, USP. Santé Canada communique ces renseignements importants sur l’innocuité aux professionnels de la santé et aux Canadiens par l’intermédiaire de la base de données des rappels et avis de sécurité sur le site Web Canadiens en santé. Cette mise à jour de communication sera distribuée par le biais du système de notification électronique MedEffetMC.
Pour signaler un problème lié à la santé ou à l’innocuité
La gestion des effets secondaires liés à un produit de santé commercialisé dépend de leur déclaration par les professionnels de la santé et les consommateurs. Tout cas d’effet indésirable grave ou imprévu chez les patients recevant la Vasopressine injectable, USP devrait être signalé à Fresenius Kabi Canada Ltd. ou à Santé Canada.
Fresenius Kabi Canada Ltd.
165 Galaxy Blvd., Suite 100, Toronto, ON, M9W 0C8, Canada
Téléphone : 1-877-779-7760
Télécopieur : 1-844-605-4465
Courriel : Canada_Vigilance@fresenius-kabi.com
Si vous avez des questions ou des préoccupations au sujet du produit autorisé aux États-Unis, la Vasopressine injectable, USP, 20 unités/mL, veuillez communiquer avec Fresenius Kabi Canada Ltd. à l’adresse Canada_medinfo@fresenius-kabi.com OU par téléphone au 1-877-779-7760.
Pour corriger votre adresse postale ou numéro de télécopieur, veuillez communiquer avec Fresenius Kabi Canada Ltd.
Vous pouvez signaler les effets secondaires soupçonnés associés à l’utilisation de produits de santé à Santé Canada :
- Composez sans frais le 1-866-234-2345; ou
- Consultez la page Web MedEffet Canada sur la déclaration des effets indésirables pour savoir comment déclarer un effet indésirable en ligne, par courrier ou par télécopieur.
Pour d’autres renseignements concernant les produits de santé reliés à cette communication, veuillez communiquer avec Santé Canada :
Direction générale des opérations réglementaires et de l’application de la loi
Courriel : hpce-cpsal@hc-sc.gc.ca
Téléphone : 1-800-267-9675
Original signé par
Prachi Chandel
Dirigeante nationale en matière de sécurité-innocuité, Gestionnaire, Vigilance et Affaires médicales
Annexe 1
A. Image du produit autorisé aux États-Unis, Vasopressine injectable, USP, 20 unités/mL, fiole
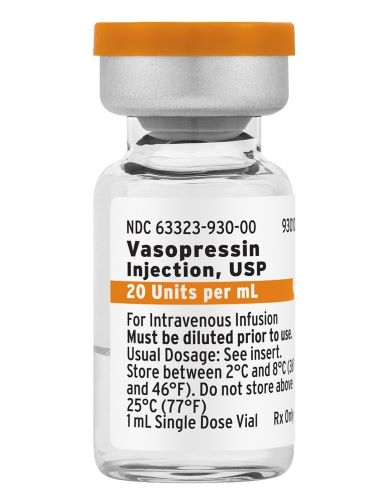
B. Image du produit autorisé aux États-Unis, Vasopressine injectable, USP, 20 unités/mL, étiquette intérieure de la fiole

|
NDC 63323-930-00 930101
Vasopressine
20 unités par mL
Pour perfusion intraveineuse Posologie habituelle : voir la notice. |
Fresnius Kabi
LOT/EXP
|
C. Image du produit autorisé aux États-Unis, Vasopressine injectable, USP, 20 unités/mL, étiquette extérieure du plateau de la boîte

|
Vasopressine 20 unités par mL Pour perfusion intraveineuse Doit être diluée avant l’utilisation Conserver entre 2 °C et 8 °C |
Sans agent de conservation Chaque mL contient : 20 unités/mL Posologie habituelle : voir la notice. Jeter les solutions pour perfusion Fresenius Kabi, Lake Zurich, IL 60047
|
Ce que vous devriez faire
Voir les messages clés ci-dessous
Renseignements supplémentaires
Détails
Recevez des notifications
Recevez des courriels concernant les nouveaux rappels et avis de sécurité, ainsi que leurs mises à jour.