Distribution de NUVAXOVID avec des étiquettes de flacons et de boîtes en anglais seulement
Résumé
Voir les messages clés ci-dessous
Produits visés
NUVAXOVID Vaccin contre la COVID-19 (protéine recombinante, avec adjuvant), 5 mcg/0,5 mL
Suspension pour injection intramusculaire, flacons multidoses.
Chaque flacon contient 10 doses (chaque dose est 0,5 mL)
DIN : 02525364
Fabricant : Novavax, Inc.
Importateur et distributeur canadien : Innomar Strategies Inc.
Problème
NUVAXOVID a été autorisé par Santé Canada le 17 février 2022. Afin de permettre un accès plus rapide à NUVAXOVID dans le contexte de la pandémie mondiale, Novavax, Inc. distribuera des flacons, des boîtes et une notice d’accompagnement en anglais seulement pendant un certain temps. Sur les étiquettes en anglais seulement du flacon et de la boîte, il manque des renseignements importants particuliers au Canada qui se trouvent normalement sur les étiquettes approuvées par Santé Canada (voir la section Information à l’intention des professionnels de la santé).
Destinataires
Professionnels de la santé, notamment les médecins spécialisés dans les maladies infectieuses, les pharmaciens, les médecins de famille, les responsables de la santé publique, les infirmières et les infirmières praticiennes.
Messages clés
- Le 17 février 2022, NUVAXOVID™ (DIN 02525364) a été autorisé par Santé Canada.
- NUVAXOVID est indiqué pour l’immunisation active dans le but de prévenir la maladie à coronavirus 2019 (COVID-19) causée par le coronavirus du syndrome respiratoire aigu sévère 2 (SRAS-CoV-2) chez les personnes âgées de 18 ans et plus.
- Afin de fournir un accès rapide à NUVAXOVID, Novavax, Inc. distribuera des flacons de produit, des boîtes et la notice d’accompagnement en anglais seulement, pendant une certaine période (voir l’annexe A).
- Les professionnels de la santé sont informés que :
- Des informations importantes spécifiques au Canada ne figurent pas sur les étiquettes des flacons et des boîtes (voir la section Information à l’intention des professionnels de la santé).
- Les informations d’étiquetage spécifiques au Canada, y compris la monographie de produit canadienne de NUVAXOVID, sont accessibles à l’adresse https://www.novavaxcovidvaccine.com/, ou en scannant le code QR sur l’étiquette de la boîte en anglais ou la notice d’accompagnement. Ces informations sont également disponibles sur le site vaccin-covid.canada.ca du gouvernement fédéral.
- La monographie de produit canadienne de NUVAXOVID, en français et en anglais, est également disponible sur la Base de données sur les produits pharmaceutiques de Santé Canada, et devrait être utilisée pour obtenir des renseignements complets sur le produit.
Contexte
NUVAXOVID est indiqué pour l’immunisation active dans le but de prévenir la maladie à coronavirus 2019 (COVID-19) causée par le coronavirus du syndrome respiratoire aigu sévère 2 (SRAS-CoV-2) chez les personnes âgées de 18 ans et plus.
Compte tenu de l’urgence de santé publique résultant de la pandémie actuelle, Santé Canada a autorisé l’importation, la vente et la publicité de NUVAXOVID avec des étiquettes de flacon et de boîte et une notice d’accompagnement en anglais seulement pour la distribution mondiale initiale du vaccin.
NUVAXOVID muni d’étiquettes internationales est le même que le NUVAXOVID autorisé par Santé Canada à tous les égards (c.-à-d., formulation, concentration, voie d’administration) et devrait être utilisé au Canada pour la même indication et selon le même calendrier de vaccination. La monographie de produit canadienne de NUVAXOVID, qui est approuvée par Santé Canada et disponible en français et en anglais, devrait être utilisée pour obtenir des renseignements complets sur le produit.
Information à l’intention des professionnels de la santé
Les professionnels de la santé sont informés que :
- La monographie de produit canadienne approuvée, qui est disponible en français et anglais sur la Base de données sur les produits pharmaceutiques de Santé Canada, sur le site Web du gouvernement fédéral vaccin-covid.canada.ca ou à https://www.novavaxcovidvaccine.com/, devrait être utilisée pour obtenir des renseignements complets sur le produit.
- Les renseignements importants suivants, propres au Canada, ne figurent pas sur les étiquettes des flacons et de la boîte :
- Numéro d’identification du médicament (DIN)
- Nom et adresse du détenteur du DIN canadien
- Nom et adresse de l’importateur et du distributeur canadien
- Tout le texte correspondant en français
- De plus, la forme posologique est indiquée comme « Dispersion for injection » et non « Suspension for intramuscular injection » (« Suspension pour injection intramusculaire » en français).
- Les informations spécifiques au Canada peuvent être consultées sur le site https://www.novavaxcovidvaccine.com/, ou en scannant le code QR figurant sur l’étiquette de la boîte ou la notice d’accompagnement. Ces informations sont également disponibles sur le site Web du gouvernement fédéral vaccin-covid.canada.ca.
- Pour toute question de nature médicale, veuillez communiquer avec le service d’information médicale au 1-855-239-9172.
Mesures prises par Santé Canada
Santé Canada permet l’utilisation d’une étiquette internationale en anglais seulement pour une période limitée. Santé Canada a imposé des conditions exigeant que Novavax, Inc. fournisse dès que possible des stocks de vaccins munis d’étiquettes spécifiques au Canada. Santé Canada a rendu accessible l’information complète sur l’étiquetage en français et en anglais sur le site Web covid-vaccine.canada.ca du gouvernement fédéral.
Santé Canada a travaillé avec Novavax, Inc. afin de préparer cette alerte pour NUVAXOVID. Santé Canada communique ces renseignements importants en matière d’innocuité aux professionnels de la santé et aux Canadiens par l’entremise de la Base de données des rappels et des alertes de sécurité sur le site Web Canadiens en santé. Cette communication sera également diffusée à travers le système de notification par courriel d’avis électronique MedEffetMC, ainsi que par les canaux de médias sociaux, notamment LinkedIn et Twitter.
Pour signaler un problème lié à la santé ou à l’innocuité
La gestion des effets secondaires liés aux produits de santé commercialisés dépend des professionnels de la santé et des consommateurs qui les signalent. Tout effet secondaire grave ou inattendu chez les patients recevant NUVAXOVID devrait être signalé à votre unité de santé locale ou à Novavax, Inc.
Novavax, Inc.
21 Firstfield Road
Gaithersburg, MD, 20878
1-855-239-9172
Pour corriger votre adresse postale ou votre numéro de télécopieur, contactez Novavax, Inc. au 1-855-239-9172.
Si un patient éprouve un effet secondaire à la suite d’une immunisation, veuillez remplir le Formulaire d’événements indésirables à la suite d’une immunisation (EIAI) approprié pour votre province/territoire et l’envoyer à votre bureau de santé local.
Pour toute autre demande de renseignements sur les produits de santé liés à cette communication, veuillez communiquer avec Santé Canada :
Direction des médicaments biologiques et radiopharmaceutiques
Courriel : brdd.dgo.enquiries@hc-sc.gc.ca
Original signé par
Henrietta Ukwu, MD
Vice-présidente principale, Chef de la réglementation
Annexe A - Étiquettes de flacons et de boîtes pour NUVAXOVID avec étiquetage en anglais seulement
Flacon
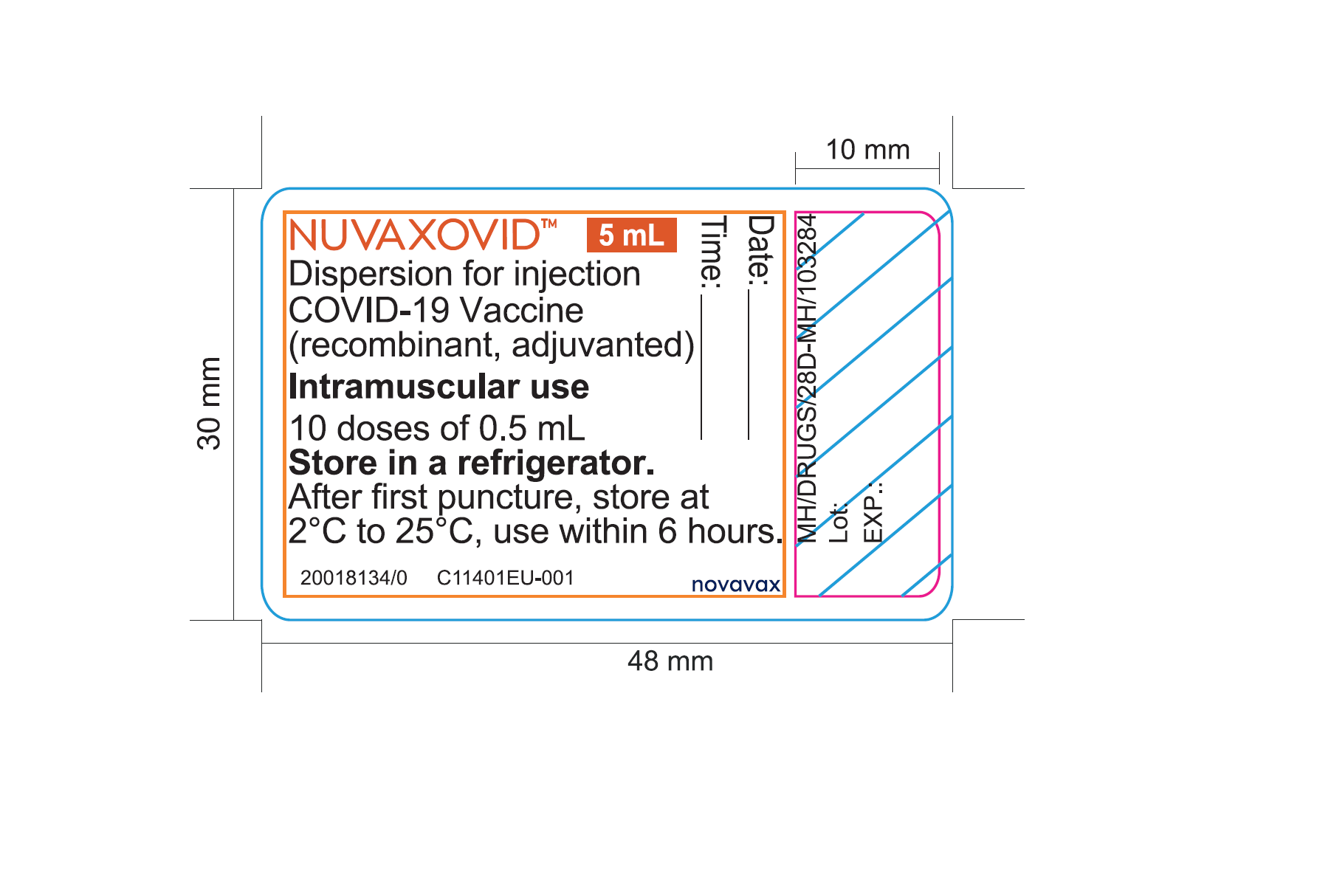
NUVAXOVID™ 5 mL
Dispersion pour injection
Vaccin contre la COVID-19 (recombinant, avec adjuvant)
Utilisation intramusculaire
10 doses de 0,5 mL
À conserver au réfrigérateur.
Après la première ponction, conserver à une température entre 2°C et 25°C, utiliser dans les 6 heures.
Novavax
Date :
Heure :
Lot :
EXP :
Boîte

Étiquette principale :
NUVAXOVID™ 5 mL
Dispersion pour injection
Vaccin contre la COVID-19 (recombinant, avec adjuvant)
Utilisation intramusculaire
10 flacons multidoses
Chaque flacon contient 10 doses de 0,5 mL
Novavax
Étiquette au dos :
Chaque dose contient 5 microgrammes de protéine spike recombinante du SRAS-CoV-2 adjuvée avec Matrix - M.
Adjuvant Matrix-M : Fraction-A et Fraction-C de l’extrait de Quillaja saponaria Molina.
Excipients : hydrogénophosphate disodique heptahydraté, dihydrogénophosphate de sodium monohydraté, hydrogénophosphate disodique dihydraté, chlorure de sodium, polysorbate 80, cholestérol, phosphatidylcholine (y compris tout-rac-α-Tocophérol) dihydrogénophosphate de potassium, chlorure de potassium, hydroxyde de sodium, acide chlorhydrique et eau pour préparations injectables.
Lire la notice d’utilisation avant de l’utiliser.
Conserver dans un réfrigérateur. Ne pas congeler.
Conserver dans l’emballage d’origine afin de protéger de la lumière.
Après la première ponction, conserver entre 2°C et 25°C, utiliser dans les 6 heures.
Étiquette latérale :
NUVAXOVID™ 5 mL
Dispersion pour injection
Vaccin contre la COVID-19 (recombinant, avec adjuvant)
Utilisation intramusculaire
[Code QR]
Pour plus d’informations, scannez ou visitez
Étiquette latérale :
NUVAXOVID™ 5 mL
Dispersion pour injection
Vaccin contre la COVID-19 (recombinant, avec adjuvant)
Utilisation intramusculaire
EU/1/21/1618/001
Novavax CZ a. s.
Bohumil 138, Jevany, 28163, République tchèque
Étiquette supérieure :
Lot :
EXP :
Code barres
Renseignements supplémentaires
Détails
Recevez des notifications
Recevez des courriels concernant les nouveaux rappels et avis de sécurité, ainsi que leurs mises à jour.