COMIRNATY (vaccin contre la COVID-19, ARNm, aussi appelé Vaccin contre la COVID-19 de Pfizer-BioNTech) : Nouvelle formulation destinée aux enfants âgés de 5 ans à moins de 12 ans
Marque(s)
Résumé
Voir les messages clés ci-dessous
Produits visés
COMIRNATY (vaccin contre la COVID-19, ARNm, aussi appelé Vaccin contre la COVID-19 de Pfizer-BioNTech)
Problème
IMPORTANT : Accès aux informations particulières relatives aux étiquettes propres au Canada durant la distribution de COMIRNATY (vaccin contre la COVID-19, ARNm, aussi appelé Vaccin contre la COVID-19 de Pfizer-BioNTech) pour les enfants âgés de 5 ans à moins de 12 ans.
Destinataires
Professionnels de la santé, à savoir médecins infectiologues, pharmaciens, médecins de famille, responsables de la santé publique, infirmières et infirmières praticiennes. Professionnels de la santé des centres de vaccination désignés.
Messages clés
- Le 19 novembre 2021, COMIRNATY (vaccin contre la COVID-19, ARNm), DIN 02522454 a reçu un avis de conformité pour une nouvelle formulation destinée aux enfants âgés de 5 ans à moins de 12 ans.
- COMIRNATY est maintenant indiqué pour l’immunisation active des personnes âgées de 5 ans et plus, afin de prévenir la maladie à coronavirus 2019 (COVID-19) causée par le coronavirus du syndrome respiratoire aigu sévère 2 (SRAS-CoV-2).
- COMIRNATY est maintenant autorisé en deux différentes formulations/présentations qui sont clairement différenciées par la couleur du capuchon (voir les annexes A et B) :
- CAPUCHON VIOLET (30 mcg/0,3 mL après dilution) : destinée aux personnes âgées de 12 ans et plus;
- CAPUCHON ORANGE (10 mcg/0,2 mL après dilution) : destinée aux enfants âgés de 5 ans à moins de 12 ans. Les étiquettes de cette formulation ont aussi une bordure orange.
- Chaque formulation est autorisée pour un groupe d’âge particulier et diffère quant aux exigences liées à l’entreposage, à la manipulation et à la préparation. Il est important de revoir attentivement ces exigences avant l’emploi (voir tableaux 1 et 2 dans la section Information à l’intention des professionnels de la santé). La formulation et le numéro de lot du vaccin doivent être inscrits dans les dossiers de vaccination des patients et à des fins de signalement d’effets secondaires.
- Les fioles de COMIRNATY destinées aux personnes âgées de 12 ans et plus (capuchon violet) ne sont pas autorisées pour la préparation des doses destinées à des enfants de 5 ans à moins de 12 ans.
- Les fioles de COMIRNATY destinées aux enfants âgés de 5 ans à moins de 12 ans (capuchon orange) doivent être jetées 12 heures après la dilution (c.-à-d. après la perforation initiale). Bien qu’il puisse être indiqué sur les étiquettes des fioles et les boîtes que la fiole doit être jetée 6 heures après la dilution, la stabilité du vaccin pendant 12 heures après la dilution a été démontrée à l’issue de tests supplémentaires.
- Bien que le nom commercial du vaccin soit désormais COMIRNATY, le Canada continuera de recevoir des fioles dont l’étiquette indiquera Vaccin contre la COVID-19 de Pfizer-BioNTech. Pfizer Canada SRI fournit des stocks de vaccin dont les boîtes et les fioles portent une étiquette unilingue anglaise avec la mention US Emergency Use Authorization afin de hâter la distribution à l’échelle mondiale de COMIRNATY.
- Les professionnels de la santé doivent être informés :
- Que des renseignements importants particuliers propres au Canada ne figurent pas sur les étiquettes de la fiole et de la boîte (voir la section Information à l’intention des professionnels de la santé).
- Que l’étiquetage du produit spécifique au Canada, à savoir la monographie de produit de COMIRNATY et le matériel de formation sont accessibles sur les sites CVDvaccine.ca/fr ou COMIRNATY.ca, ou en balayant le code QR figurant sur l’étiquette unilingue anglaise de la boîte. Ces renseignements sont également accessibles sur le site Web du gouvernement fédéral vaccin-covid.canada.ca. Que la monographie canadienne du produit est également accessible en français et en anglais dans la Base de données sur les produits pharmaceutiques de Santé Canada ou sur le site de pfizer.ca.
Quel est le problème?
Le 16 septembre 2021, un avis de conformité initial a été émis pour COMIRNATY (vaccin contre la COVID-19, ARNm) en vertu du Règlement sur les aliments et drogues, en remplacement de l’autorisation préalable accordée en vertu d’un arrêté d’urgence.
Le 19 novembre 2021, COMIRNATY (vaccin contre la COVID-19, ARNm) a également reçu un avis de conformité pour une nouvelle formulation (DIN 02522454) destinée aux enfants âgés de 5 ans à moins de 12 ans.
À titre de mesure exceptionnelle, afin d’offrir un accès plus rapide aux stocks de vaccin dans le contexte de la pandémie mondiale, Pfizer et BioNTech continuent de fournir des stocks de vaccin dans des boîtes et des fioles dont l’étiquette porte le nom Vaccin contre la COVID-19 de Pfizer-BioNTech. Sur ces étiquettes unilingues anglaises, il manque des renseignements importants particuliers au Canada qui se trouvent normalement sur les étiquettes approuvées par Santé Canada (voir la section Information à l’intention des professionnels de la santé).
Produits visés
COMIRNATY (vaccin contre la COVID-19, ARNm, aussi appelé Vaccin contre la COVID-19 de Pfizer-BioNTech) pour les enfants de 5 ans à < 12 ans, suspension pour injection intramusculaire, fioles multidoses. Chaque fiole contient 10† doses (de 0,2 mL chacune).
DIN : 02522454
Fabricant : BioNTech Manufacturing GmbH (Allemagne)
Importateur et distributeur canadien : Pfizer Canada SRI
† Des seringues et/ou des aiguilles à faible volume mort peuvent être utilisées pour prélever 10 doses dans chaque fiole. En utilisant des seringues et des aiguilles standards, le volume pourrait être insuffisant pour permettre le prélèvement de 10 doses à partir d’une même fiole.
Contexte
COMIRNATY est maintenant offert en deux différentes formulations et présentations autorisées et nettement différenciées au moyen de la couleur du capuchon de la fiole. Les fioles destinées aux enfants âgés de 5 ans à moins de 12 ans ont un capuchon orange et les étiquettes des fioles ont une bordure orange.
Compte tenu de l’urgence de santé publique causée par la pandémie actuelle, Santé Canada a autorisé l’importation, la vente et la publicité de COMIRNATY destiné aux enfants âgés de 5 ans à < 12 ans dans des boîtes et des fioles dont les étiquettes sont en anglais seulement et qui sont destinées à la distribution mondiale actuelle du vaccin.
En ce qui concerne tous les autres aspects du vaccin destiné aux enfants âgés de 5 ans à < 12 ans avec des étiquettes en anglais seulement (c.-à-d. formulation, teneur, voie d’administration), il n’y a aucune différence par rapport à COMIRNATY destiné aux enfants âgés de 5 ans à < 12 ans qui a été autorisé par Santé Canada. Il faut utiliser la monographie de produit canadienne de COMIRNATY, qui est approuvée par Santé Canada et accessible en français et en anglais, pour connaître les renseignements complets sur le produit.
Information à l’intention des professionnels de la santé
COMIRNATY est maintenant offert en deux différentes formulations et présentations autorisées (voir les annexes A et B) :
- Personnes âgées de 12 ans et plus : capuchon violet
- Enfants âgés de 5 ans à moins de 12 ans : capuchon orange avec étiquette à bordure orange
IMPORTANT : Chaque formulation est autorisée pour un groupe d’âge particulier et diffère quant aux exigences liées à l’entreposage, à la manipulation et à la préparation. Ces différences sont présentées dans le tableau 1 ci-dessous, et il est important d’en prendre note attentivement avant l’emploi. La formulation et le numéro de lots doivent être inscrits dans les dossiers de vaccination des patients et à des fins de signalement d’effets secondaires.
Le vaccin contenu dans la fiole portant l’étiquette « DILUER AVANT UTILISATION 5 ans à < 12 ans » (en anglais : “DILUTE PRIOR TO USE Age 5y to <12y”) devrait être utilisé pour la vaccination des enfants âgés de 5 ans à moins de 12 ans (capuchon orange).
Les fioles de COMIRNATY destinées aux personnes âgées de 12 ans et plus (capuchon violet) ne sont pas autorisées pour la préparation des doses destinées à des enfants de 5 ans à moins de 12 ans. Les personnes âgées de 12 ans et plus peuvent continuer de recevoir la présentation avec le capuchon violet.
Tableau 1: Différences importantes entre les 2 formulations/présentations de COMIRNATY1
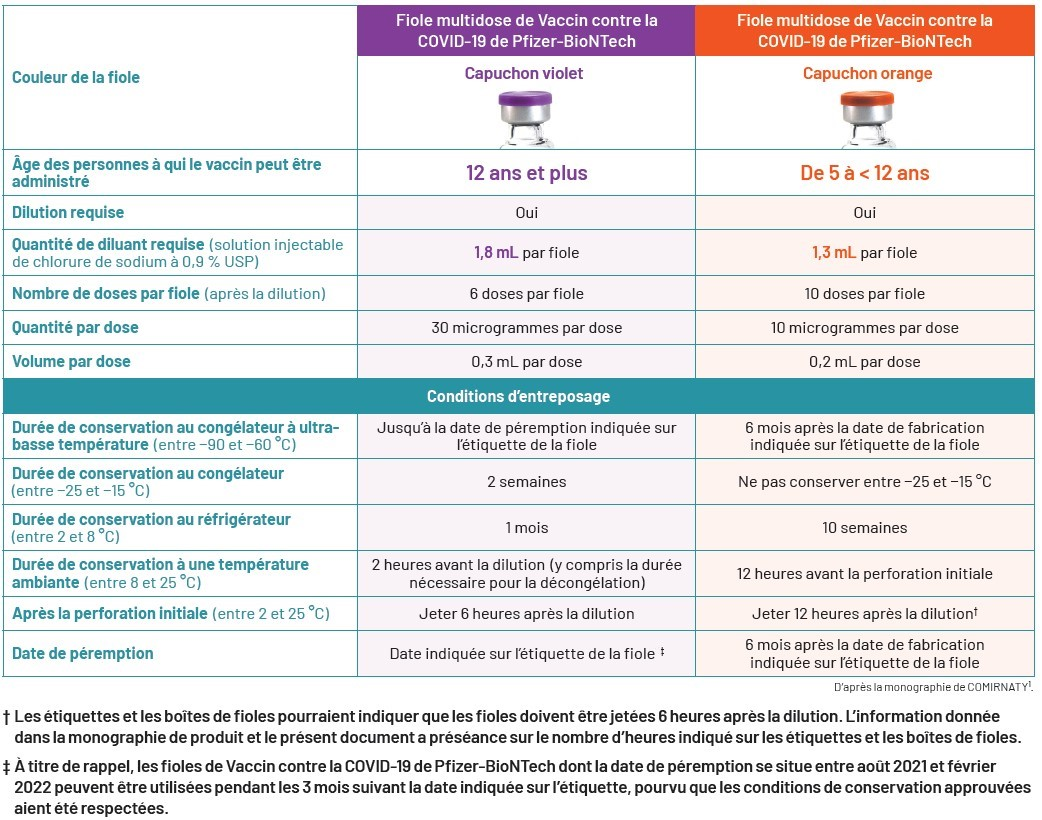
Rappels importants concernant le tableau 1 ci-dessus :
- UTILISER UNIQUEMENT une solution injectable stérile de chlorure de sodium à 0,9 % USP comme diluant.
- Formulation pour enfants âgés de 5 ans à < 12 ans (capuchon orange) : quelles que soient les conditions de conservation, les vaccins ne doivent pas être utilisés après 6 mois à compter de la date de fabrication imprimée sur chaque fiole ainsi que sur les boîtes.
- Comme l’information ci-dessus peut changer, toujours consulter CVDvaccine.ca ou COMIRNATY.ca pour les renseignements les plus récents.
Les conditions d’entreposage à long terme établies pour COMIRNATY pour enfants âgés de 5 ans à < 12 ans sont de 6 mois à une température variant entre −90 °C et −60 °C. Les étiquettes ne portent pas de date de péremption. À leur réception, les fioles congelées peuvent être immédiatement placées dans un réfrigérateur pour être décongelées et conservées pour une durée maximale de 10 semaines. La date de péremption des 10 semaines au réfrigérateur doit être inscrite sur la boîte au moment où celle-ci est transférée au réfrigérateur. Le vaccin ne doit pas être utilisé après 6 mois à compter de la date de fabrication imprimée sur la fiole et la boîte, comme l’illustre le tableau ci-dessous (également disponible sur CVDvaccine.ca et COMIRNATY.ca) :
Tableau 2 : Renseignements sur la date de péremption de COMIRNATY pour enfants âgés de 5 ans à <12 ans
Les fioles de COMIRNATY pour enfants âgés de 5 à<12 ans (capuchon orange) doivent être jetées 12 heures après la dilution (c.-à-d. après la perforation initiale). Bien qu’il puisse être indiqué sur les étiquettes des fioles et les boîtes que la fiole doit être jetée 6 heures après la dilution, la stabilité du vaccin pendant 12 heures après la dilution a été démontrée à l’issue de tests supplémentaires. L’information incluse dans la monographie de produit et la présente communication a préséance sur la mention imprimée sur les étiquettes et les boîtes de fioles concernant le nombre d’heures après lesquelles les fioles doivent être jetées.
Tel que nous l’avons mentionné précédemment, dans le but d’offrir à la population canadienne un accès rapide à COMIRNATY, Pfizer et BioNTech continueront, pour l’instant, de fournir le produit dans des fioles et des boîtes portant des étiquettes en anglais seulement.
Les professionnels de la santé doivent être informés :
- Que les renseignements particuliers au Canada sont accessibles sur les sites CVDvaccine.ca/fr ou COMIRNATY.ca, ou en balayant le code QR figurant sur l’étiquette de la boîte. Ces renseignements sont également accessibles sur le site Web du gouvernement fédéral vaccin-covid.canada.ca. Que la monographie canadienne du produit est également accessible en français et en anglais dans la Base de données sur les produits pharmaceutiques de Santé Canada ou sur le site de pfizer.ca.
- Que les renseignements importants suivants particuliers au Canada ne figurent pas sur les étiquettes de la fiole et de la boîte.
- Numéro d’identification du médicament (DIN)
- Nom et adresse du titulaire du DIN au Canada
- Nom et adresse de l’importateur et du distributeur canadien
- Ensemble du texte correspondant en français
- La marque de commerce COMIRNATY
- Qu’afin de fournir les stocks actuels du vaccin, les étiquettes de la fiole et/ou de la boîte comportent les énoncés For use under Emergency Use Authorization. Que les renseignements spécifiques à la Food and Drug Administration des États-Unis (p. ex., Rx only, NDC) doivent être ignorés, car ils ne sont pas pertinents à l’autorisation canadienne.
- Pour toute question de nature médicale, de communiquer avec le Service de l’information pharmaceutique de Pfizer Canada SRI au 1-800-463-6001.
- Pour toute autre question d’ordre général, de communiquer avec le Service à la clientèle de Pfizer Canada SRI au 1-833-VAX-COVI (1-833-829-2684) ou par courriel au CanadaCSVaccine@pfizer.com
Mesures prises par Santé Canada
Santé Canada permet pour une période limitée l’utilisation de l’étiquette unilingue anglaise qui reflète l’utilisation d’urgence aux États-Unis. Santé Canada a imposé des conditions exigeant que Pfizer Canada SRI fournisse dès que possible des stocks de vaccin portant les étiquettes particulières au Canada. Santé Canada a rendu accessible tout l’étiquetage en français et en anglais sur le site Web du gouvernement fédéral vaccin-covid.canada.ca.
Santé Canada communique aux professionnels de la santé et aux Canadiens ces renseignements importants relatifs à l’innocuité par l’intermédiaire de la base de données des rappels et avis de sécurité sur le site Web de Canadiens en santé. Cette communication sera également diffusée au moyen du système de notification d’avis électronique de MedEffetMC, de même que dans les médias sociaux, notamment LinkedIn et Twitter.
Pour signaler un problème lié à la santé ou à l’innocuité
La gestion des effets secondaires liés à un produit de santé commercialisé dépend de leur déclaration par les professionnels de la santé et les consommateurs. Tout effet secondaire grave ou imprévu chez les patients recevant COMIRNATY doit être signalé à Pfizer Canada SRI ou à votre unité de santé locale.
Pfizer Canada SRI
17300, autoroute Transcanadienne
Kirkland (Québec)
H9J 2M5
www.pfizerdeclarationeffetindesirable.com
Télécopieur : 1-855-242-5652
Pour corriger votre adresse postale ou numéro de télécopieur, veuillez communiquer avec le Service à la clientèle de Pfizer Canada SRI au 1-833-VAX-COVI (1-833-829-2684).
Si un patient présente un effet secondaire après avoir reçu un vaccin, veuillez remplir le Formulaire de rapport des effets secondaires suivant l’immunisation (ESSI) approprié à votre province ou territoire (https://www.canada.ca/fr/sante-publique/services/immunisation/declaration-manifestations-cliniques-inhabituelles-suite-immunisation/formulaire.html) et l’envoyer à votre unité de santé locale.
Pour d’autres renseignements concernant les produits de santé reliés à cette communication, veuillez communiquer avec Santé Canada :
Direction des médicaments biologiques et radiopharmaceutiques
Courriel : brdd.dgo.enquiries@hc-sc.gc.ca
Document original signé par
Vratislav Hadrava, M.D., Ph. D.
Vice-président et directeur médical
Pfizer Canada SRI
Référence
- COMIRNATY (vaccin contre la COVID-19, ARNm) [monographie de produit]. Mayence (Allemagne): BioNTech Manufacturing GmbH; 2021.
Annexe A
|
COMIRNATY (Vaccin contre la COVID-19 de Pfizer-BioNTech) pour les enfants de 5 ans à < 12 ans
Étiquettes unilingues anglaises de la fiole et de la boîte |
FIOLE (capuchon orange)
BOÎTE (10-fioles)
Panneau avant


Annexe B
|
COMIRNATY (Vaccin contre la COVID-19 de Pfizer-BioNTech) pour les personnes de 12 ans et plus
Étiquettes unilingues anglaises de la fiole et de la boîte |
FIOLE (capuchon violet)
Boîte (195-fioles)
Renseignements supplémentaires
Détails
Recevez des notifications
Recevez des courriels concernant les nouveaux rappels et avis de sécurité, ainsi que leurs mises à jour.