COMIRNATY Original & Omicron BA.4/BA.5, vaccin bivalent, offert dans une boîte et une fiole munies d’étiquettes unilingues anglaises : nouvelle présentation destinée aux enfants âgés de 5 ans à < 12 ans
Résumé
Voir les messages clés ci-dessous
Produits visés
COMIRNATY Original & Omicron BA.4/BA.5 (vaccin à ARNm contre la COVID-19, bivalent [souche originale et variant Omicron BA.4/BA.5]) destiné aux enfants âgés de 5 ans à < 12 ans, suspension pour injection intramusculaire, fioles multidoses. Chaque fiole dosée à 10 mcg/0,2 mL – À DILUER AVANT L’ADMINISTRATION – munie d’un CAPUCHON ORANGE et d’une ÉTIQUETTE À BORDURE ORANGE, contient 10 doses[1] de 0,2 mL après la dilution.
DIN : 02533197
Fabricant : BioNTech Manufacturing GmbH (Allemagne)
Importateur et distributeur canadien : Pfizer Canada SRI
[1] Des seringues et/ou des aiguilles à faible volume mort peuvent être utilisées pour prélever 10 doses dans chaque fiole. En utilisant des seringues et des aiguilles standards, le volume pourrait être insuffisant pour permettre le prélèvement de 10 doses à partir d’une même fiole.
Problème
Le 9 décembre 2022, Santé Canada a homologué une nouvelle présentation de COMIRNATY Original & Omicron BA.4/BA.5, vaccin bivalent, comme dose de rappel pour l’immunisation active des enfants âgés de 5 ans à < 12 ans contre la maladie à coronavirus 2019 (COVID-19) causée par le coronavirus du syndrome respiratoire aigu sévère 2 (SRAS-CoV-2).
Afin d’offrir un accès rapide à la nouvelle présentation, Pfizer Canada SRI distribuera pendant un certain temps des fioles et des boîtes portant une étiquette unilingue anglaise avec la mention « Pfizer-BioNTech COVID-19 Vaccine, Bivalent Original and Omicron BA.4/BA.5 ». Des renseignements importants propres au Canada ne figurent pas sur ces étiquettes (voir la section Information à l’intention des professionnels de la santé).
Le vaccin bivalent COMIRNATY Original & Omicron BA.4/BA.5 (DIN : 02533197) est présenté dans une fiole munie d’un CAPUCHON ORANGE et d’une ÉTIQUETTE À BORDURE ORANGE, tout comme le vaccin monovalent COMIRNATY (vaccin contre la COVID-19, ARNm), 10 mcg/0,2 mL (DIN : 02522454). Il faut accorder une attention particulière à l’étiquette de la fiole et de la boîte afin d’éviter des erreurs de médicament.
Destinataires
Professionnels de la santé, à savoir médecins infectiologues, pharmaciens, médecins de famille, responsables de la santé publique, personnel infirmier et autres professionnels de la santé des centres de vaccination.
Messages clés
- Le 9 décembre 2022, Santé Canada a homologué une nouvelle présentation de COMIRNATY Original & Omicron BA.4/BA.5 (vaccin à ARNm contre la COVID-19, bivalent [souche originale et variant Omicron BA.4/BA.5]; DIN : 02533197) destinée aux enfants âgés de 5 ans à < 12 ans.
- La nouvelle présentation est indiquée comme dose de rappel pour l’immunisation active des enfants âgés de 5 ans à < 12 ans contre la maladie à coronavirus 2019 (COVID-19) causée par le coronavirus du syndrome respiratoire aigu sévère 2 (SRAS-CoV-2).
- Afin d’offrir un accès rapide à la nouvelle présentation, Pfizer Canada SRI distribuera pendant un certain temps des fioles et des boîtes portant une étiquette unilingue anglaise avec la mention « Pfizer-BioNTech COVID-19 Vaccine, Bivalent Original and Omicron BA.4/BA.5 » (voir l’annexe A).
- Les stocks existants du vaccin monovalent COMIRNATY (vaccin contre la COVID-19, ARNm, aussi appelé Vaccin contre la COVID-19 de Pfizer-BioNTech), 10 mcg/0,2 mL, destiné aux enfants de 5 ans à < 12 ans, sont toujours disponibles.
- Les professionnels de la santé doivent être informés de ce qui suit :
- Le vaccin bivalent COMIRNATY Original & Omicron BA.4/BA.5 (DIN : 02533197) est présenté dans une fiole munie d’un CAPUCHON ORANGE et d’une ÉTIQUETTE À BORDURE ORANGE, tout comme le vaccin monovalent COMIRNATY (vaccin contre la COVID-19, ARNm), 10 mcg/0,2 mL (DIN : 02522454). Il faut accorder une attention particulière à l’étiquette de la fiole et de la boîte afin d’éviter des erreurs de médicament.
- Des renseignements importants propres au Canada ne figurent pas sur les étiquettes de la fiole et de la boîte (voir la section Information à l’intention des professionnels de la santé).
- Le libellé du produit propre au Canada, à savoir la monographie de COMIRNATY Original & Omicron BA.4/BA.5 et le matériel de formation, sont accessibles sur le site cvdvaccine.ca/fr ou en balayant le code QR figurant sur l’étiquette unilingue anglaise de la boîte. Ces renseignements sont également accessibles sur le site Web du gouvernement fédéral au vaccin-covid.canada.ca. La monographie canadienne de COMIRNATY Original & Omicron BA.4/BA.5, en français et en anglais, est également accessible dans la Base de données sur les produits pharmaceutiques de Santé Canada et au pfizer.ca/fr.
Contexte
La nouvelle présentation de COMIRNATY Original & Omicron BA.4/BA.5 (vaccin à ARNm contre la COVID-19, bivalent [souche originale et variant Omicron BA.4/BA.5]) est indiquée comme dose de rappel pour l’immunisation active des enfants âgés de 5 ans à < 12 ans contre la maladie à coronavirus 2019 (COVID-19) causée par le coronavirus du syndrome respiratoire aigu sévère 2 (SRAS-CoV-2).
Compte tenu de l’urgence de santé publique causée par la pandémie actuelle, Santé Canada a autorisé l’importation, la vente et la publicité de la nouvelle présentation de COMIRNATY Original & Omicron BA.4/BA.5 dans des boîtes et des fioles dont les étiquettes sont en anglais seulement, destinées à la distribution mondiale initiale du vaccin, et sur lesquelles apparaît le nom « Pfizer-BioNTech COVID-19 Vaccine, Bivalent Original and Omicron BA.4/BA.5 ».
Il faut utiliser la monographie canadienne du vaccin bivalent COMIRNATY Original & Omicron BA.4/BA.5, qui est approuvée par Santé Canada et accessible en français et en anglais, pour connaître les renseignements complets sur le produit.
Information à l’intention des professionnels de la santé
Les professionnels de la santé doivent être informés de ce qui suit :
- Le 9 décembre 2022, Santé Canada a homologué une nouvelle présentation de COMIRNATY Original & Omicron BA.4/BA.5 (vaccin à ARNm contre la COVID‑19, bivalent [souche originale et variant Omicron BA.4/BA.5]; DIN : 02533197) comme dose de rappel pour les enfants âgés de 5 ans à < 12 ans.
- Afin d’offrir un accès rapide à la nouvelle présentation, Pfizer Canada SRI distribuera pendant un certain temps des fioles et des boîtes portant une étiquette unilingue anglaise avec la mention « Pfizer-BioNTech COVID-19 Vaccine, Bivalent Original and Omicron BA.4/BA.5 » (voir l’annexe A).
- Les stocks existants du vaccin monovalent COMIRNATY (vaccin contre la COVID-19, ARNm, aussi appelé Vaccin contre la COVID-19 de Pfizer-BioNTech), 10 mcg/0,2 mL, destiné aux enfants de 5 ans à < 12 ans, sont toujours disponibles.
- Le vaccin bivalent COMIRNATY Original & Omicron BA.4/BA.5 (DIN : 02533197) est présenté dans une fiole munie d’un CAPUCHON ORANGE et d’une ÉTIQUETTE À BORDURE ORANGE, tout comme le vaccin monovalent COMIRNATY (vaccin contre la COVID-19, ARNm), 10 mcg/0,2 mL (DIN : 02522454). Il faut accorder une attention particulière à l’étiquette de la fiole et de la boîte afin d’éviter des erreurs de médicament.
- Le libellé du produit propre au Canada, à savoir la monographie de COMIRNATY Original & Omicron BA.4/BA.5 et le matériel de formation, sont accessibles sur le site cvdvaccine.ca/fr ou en balayant le code QR figurant sur l’étiquette unilingue anglaise de la boîte. Ces renseignements sont également accessibles sur le site Web du gouvernement fédéral au vaccin-covid.canada.ca. La monographie canadienne de COMIRNATY Original & Omicron BA.4/BA.5, en français et en anglais, est également accessible dans la Base de données sur les produits pharmaceutiques de Santé Canada ou au pfizer.ca/fr.
- Les renseignements importants suivants propres au Canada ne figurent pas sur les étiquettes de la fiole et de la boîte :
- Numéro d’identification du médicament (DIN)
- Nom et adresse du titulaire du DIN au Canada
- Nom et adresse de l’importateur et du distributeur canadien
- Ensemble du texte correspondant en français
- Nom sous lequel le vaccin est commercialisé au Canada : « COMIRNATY Original & Omicron BA.4/BA.5 »
- Les étiquettes de la fiole et de la boîte des stocks actuels du vaccin comportent l’énoncé « For use under Emergency Use Authorization » (Autorisation pour une utilisation d’urgence). Les renseignements spécifiques de la Food and Drug Administration (FDA) des États-Unis (p. ex., Rx only, NDC) doivent être ignorés, car ils ne sont pas pertinents à l’autorisation canadienne.
- Pour toute question de nature médicale, il faut communiquer avec le Service de l’information pharmaceutique de Pfizer Canada SRI au 1-800-463-6001.
- Pour toute autre question d’ordre général, il faut communiquer avec le Service à la clientèle de Pfizer Canada SRI au 1-833-VAX-COVI (1-833-829-2684) ou par courriel au CanadaCSVaccine@pfizer.com.
Mesures prises par Santé Canada
Santé Canada permet l’utilisation de l’étiquette unilingue anglaise pour une période limitée. Santé Canada a imposé des conditions exigeant que Pfizer Canada SRI fournisse dès que possible des stocks de vaccin portant les étiquettes propres au Canada. Santé Canada a rendu accessible tout l’étiquetage en français et en anglais sur le site Web du gouvernement fédéral au vaccin-covid.canada.ca.
Santé Canada communique aux professionnels de la santé et aux Canadiens ces renseignements importants relatifs à l’innocuité par l’intermédiaire de la Base de données des rappels et avis de sécurité sur le site Web de Canadiens en santé. Cette communication sera également diffusée au moyen du système de notification d’avis électronique de MedEffetMC, de même que dans les médias sociaux, notamment LinkedIn et Twitter.
Pour signaler un problème lié à la santé ou à l’innocuité
La gestion des effets secondaires liés à un produit de santé commercialisé dépend de leur déclaration par les professionnels de la santé et les consommateurs. Tout effet secondaire grave ou imprévu chez les patients recevant COMIRNATY Original & Omicron BA.4/BA.5 doit être signalé à votre unité de santé locale ou à Pfizer Canada SRI.
Pfizer Canada SRI
17300, autoroute Transcanadienne
Kirkland (Québec)
H9J 2M5
www.pfizerdeclarationeffetindesirable.com
Téléphone : 1-866-723-7111
Télécopieur : 1-855-242-5652
Pour corriger votre adresse postale ou numéro de télécopieur, veuillez communiquer avec le Service à la clientèle de Pfizer Canada SRI au 1‑833‑VAX‑COVI (1-833-829-2684).
Si un patient présente un effet secondaire après avoir reçu un vaccin, veuillez remplir le Formulaire de rapport des effets secondaires suivant l’immunisation (ESSI) approprié à votre province ou territoire et l’envoyer à votre unité de santé locale.
Pour d’autres renseignements concernant les produits de santé reliés à cette communication, veuillez communiquer avec Santé Canada :
Direction des médicaments biologiques et radiopharmaceutiques
Courriel : brdd.dgo.enquiries@hc-sc.gc.ca
Document original signé par
Vratislav Hadrava, M.D., Ph. D.
Vice-président et directeur médical
Pfizer Canada SRI
Annexe A – Étiquettes unilingues anglaises de la fiole et de la boîte de COMIRNATY Original & Omicron BA.4/BA.5 (vaccin à ARNm contre la COVID-19, bivalent [souche originale et variant Omicron BA.4/BA.5]) pour les enfants âgés de 5 ans à < 12 ans
Étiquette de la fiole*

Traduction de l’étiquette de la fiole

* L’étiquette peut varier selon la chaîne d’approvisionnement du produit, et présenter les différences mineures suivantes :
- Le code de composant de l’étiquette pourrait être différent.
- Une bande verte pourrait être présente près de la bordure orange inférieure de l’étiquette.
Étiquette de la boîte† (10 fioles)
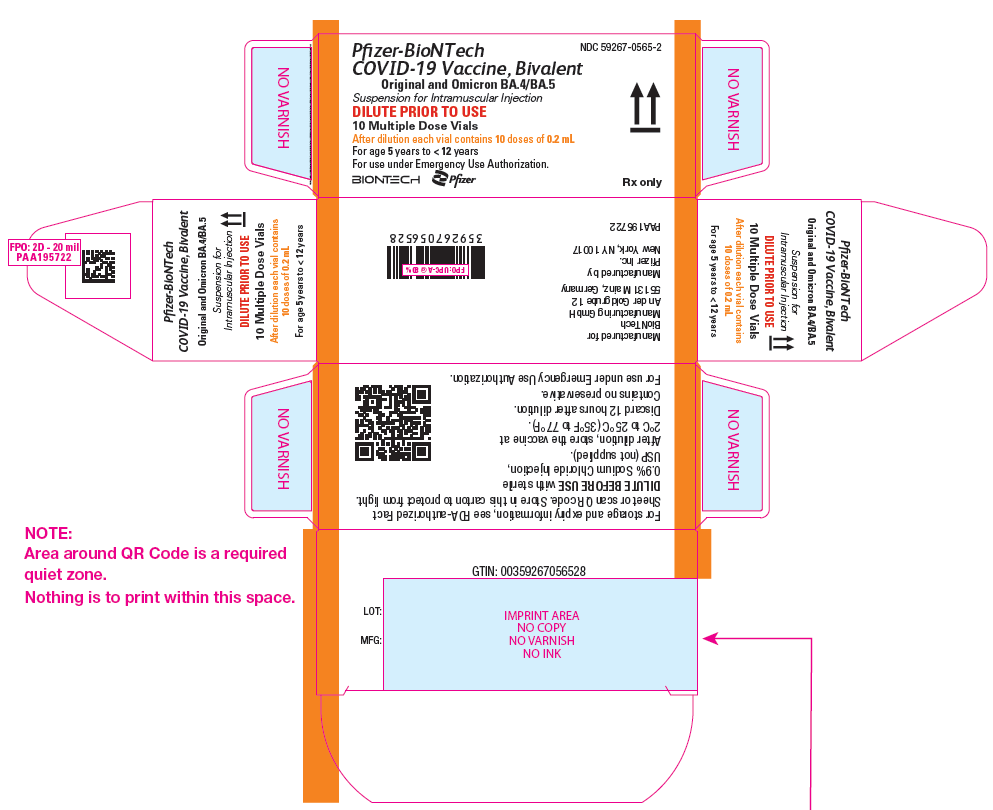

Renseignements supplémentaires
Détails
Recevez des notifications
Recevez des courriels concernant les nouveaux rappels et avis de sécurité, ainsi que leurs mises à jour.